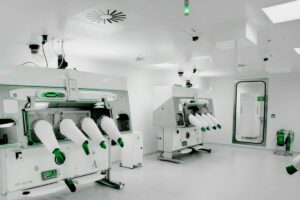
Cleanroom – Proses validasi ruang bersih atau clean room sangat penting dalam industri yang membutuhkan lingkungan steril dan terkendali, seperti farmasi, makanan, dan perangkat medis. Validasi ruang bersih memastikan bahwa lingkungan produksi aman, bersih, dan memenuhi standar yang telah ditetapkan, sehingga produk yang dihasilkan berkualitas tinggi dan aman untuk digunakan konsumen. Berikut ini adalah langkah-langkah dalam proses validasi ruang bersih yang perlu dilakukan untuk memastikan ruangan memenuhi persyaratan operasional.
1. Menentukan Rencana Validasi
Langkah pertama yang krusial dalam proses validasi ruang bersih adalah menyusun Rencana Validasi yang komprehensif. Rencana ini akan berperan sebagai panduan utama dan peta jalan dari setiap tahapan validasi. Di dalam rencana ini, kita perlu menjelaskan tujuan validasi, cakupan proses, kriteria penerimaan, serta perincian aktivitas dan waktu pelaksanaannya.
Misalnya, jika ruang bersih digunakan untuk memproduksi obat-obatan, maka rencana validasi harus merujuk pada standar-standar internasional, seperti Good Manufacturing Practice (GMP) dan ISO 14644, untuk memastikan lingkungan memenuhi batas partikel dan mikroorganisme tertentu. Rencana yang baik juga perlu mencakup strategi mitigasi apabila ada temuan selama proses validasi yang tidak sesuai.
2. Melakukan Penilaian Risiko
Selanjutnya adalah melakukan penilaian risiko atau risk assessment. Ini adalah langkah penting untuk mengidentifikasi dan menganalisis potensi ancaman terhadap keamanan produk dan kesehatan pengguna yang mungkin ditimbulkan oleh ruang bersih. Risiko yang teridentifikasi akan menentukan area mana yang perlu diperhatikan dengan lebih saksama, serta prioritas aktivitas validasi yang perlu dilakukan.
Misalnya, jika terdapat risiko tinggi terhadap kontaminasi udara di area produksi, maka pengujian aliran udara, jumlah partikel, dan filtrasi udara harus dilakukan secara ketat. Dengan memprioritaskan penilaian ini, kita dapat memastikan bahwa tindakan pencegahan dilakukan pada area yang benar-benar membutuhkan perhatian khusus.
3. Melaksanakan Kualifikasi Instalasi
Langkah ketiga adalah Kualifikasi Instalasi atau Installation Qualification (IQ), yang bertujuan memastikan semua peralatan di ruang bersih telah terpasang dengan benar sesuai spesifikasi. Kualifikasi ini mencakup pengujian kalibrasi, verifikasi peralatan, pemeriksaan dokumen, serta pemantauan infrastruktur ruangan dan peralatannya.
Dalam proses IQ, setiap komponen yang ada di ruang bersih, seperti sistem HVAC, filter HEPA, lampu UV, dan sensor suhu, diperiksa dan diuji agar sesuai standar operasional. Selain itu, data terkait kalibrasi peralatan juga harus dicatat dan dilaporkan. Langkah ini memastikan bahwa peralatan di ruang bersih siap untuk digunakan dalam tahap-tahap validasi selanjutnya.
4. Melaksanakan Kualifikasi Operasional (OQ)
Setelah IQ, tahap berikutnya adalah Kualifikasi Operasional atau Operational Qualification (OQ). Tahap ini menguji kinerja peralatan di dalam ruang bersih untuk memastikan bahwa semuanya bekerja sesuai dengan batasan atau spesifikasi yang telah ditetapkan. Beberapa pengujian utama dalam OQ meliputi pengukuran aliran udara, monitoring jumlah partikel di udara, pengaturan suhu dan kelembaban, serta uji tekanan ruangan.
Kualifikasi operasional penting untuk melihat apakah ruang bersih dapat mempertahankan standar kualitas dalam kondisi operasional normal. Misalnya, jumlah partikel di udara yang dihasilkan oleh sistem filtrasi perlu diuji untuk memastikan bahwa tidak ada kontaminasi yang bisa merusak produk.
5. Melaksanakan Kualifikasi Kinerja (PQ)
Tahapan selanjutnya adalah Kualifikasi Kinerja atau Performance Qualification (PQ). PQ melibatkan pengujian dan pemantauan kinerja ruang bersih dalam kondisi produksi aktual. Pada tahapan ini, ruang bersih diuji dalam berbagai skenario produksi untuk memvalidasi kinerja yang konsisten dan andal.
Selama PQ, pemantauan dilakukan secara berkelanjutan untuk memastikan tidak ada penyimpangan dalam kondisi ruang bersih, seperti lonjakan jumlah partikel atau fluktuasi suhu. Langkah ini membantu memastikan bahwa lingkungan tetap steril dan memenuhi standar kualitas saat ruang bersih digunakan untuk produksi nyata.
Baca juga Pentingnya Validasi Ruang Bersih untuk Menjamin Kebersihan dan Keamanan Produk
6. Dokumentasi dan Pelaporan
Langkah terakhir dalam proses validasi ruang bersih adalah melakukan dokumentasi dan pelaporan yang rinci. Semua kegiatan validasi, termasuk hasil pengujian, penyimpangan yang ditemukan, dan tindakan perbaikan, harus didokumentasikan secara terperinci. Dokumentasi ini penting tidak hanya sebagai bukti bahwa ruang bersih telah divalidasi, tetapi juga sebagai referensi untuk audit dan perbaikan berkelanjutan.
Laporan validasi perlu mencakup temuan dan rekomendasi untuk perbaikan, serta analisis terhadap hasil yang diperoleh selama proses validasi. Dokumentasi yang baik akan memudahkan perusahaan dalam melakukan kualifikasi ulang secara berkala dan memenuhi persyaratan dari pihak regulator.
Proses validasi ruang bersih adalah upaya penting untuk memastikan lingkungan produksi yang aman, steril, dan sesuai standar. Mulai dari perencanaan, penilaian risiko, hingga kualifikasi instalasi, operasional, kinerja, dan dokumentasi, setiap langkah memiliki peran penting dalam menjamin bahwa ruang bersih mampu mendukung produksi yang berkualitas tinggi.
Proses ini tidak hanya meningkatkan kualitas produk, tetapi juga melindungi keselamatan konsumen dan menjaga reputasi perusahaan. Dengan melakukan validasi ruang bersih yang benar, kita dapat mengurangi risiko, meningkatkan kepercayaan pelanggan, dan memastikan bahwa standar kualitas selalu tercapai.